Tải giáo án Powerpoint Hoá học 11 cánh diều Bài 19: Carboxylic acid
Tải bài giảng điện tử powerpoint Hóa học 11 cánh diều Bài 19: Carboxylic acid. Bài học được thiết kể đẹp mắt, nội dung giảng dạy hay nhiều trò chơi và video phong phú thu hút học sinh tập trung nắm bắt kiến thức quan trong. Tải giáo án Powerpoint Powerpoint tải về chỉnh sửa được. Kéo xuống để xem chi tiết
Rõ nét về file powerpoint trình chiếu. => Xem thêm
CHÀO MỪNG CẢ LỚP QUAY TRỞ LẠI MÔN HỌC!
KHỞI ĐỘNG
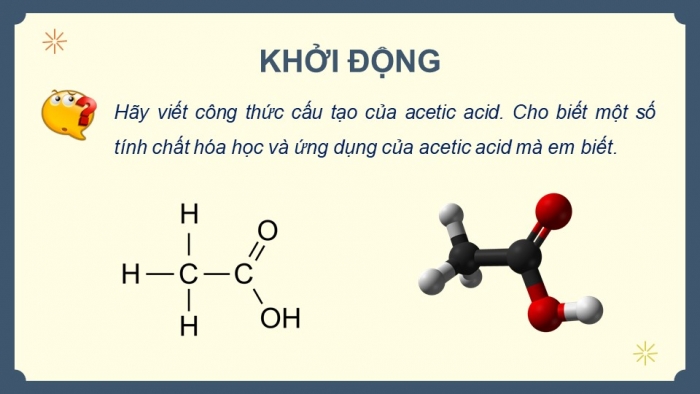
Hãy viết công thức cấu tạo của acetic acid. Cho biết một số tính chất hóa học và ứng dụng của acetic acid mà em biết.
BÀI 19: CARBOXYLIC ACID
NỘI DUNG BÀI HỌC
- KHÁI NIỆM VÀ DANH PHÁP
- Khái niệm
Thảo luận nhóm đôi
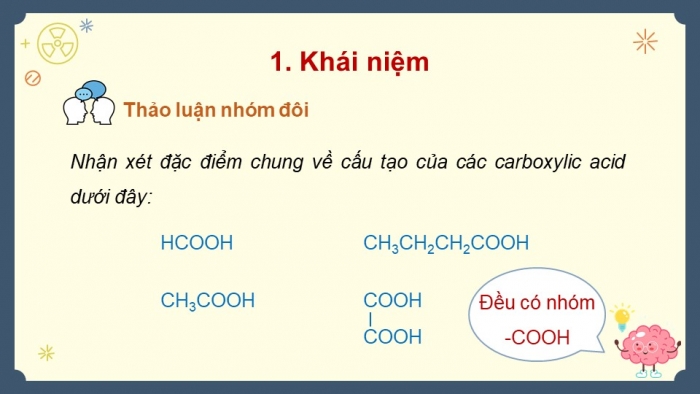
Nhận xét đặc điểm chung về cấu tạo của các carboxylic acid dưới đây:
Em hãy rút ra khái niệm và công thức chung của carboxylic acid no, đơn chức, mạch hở.
Khái niệm
Carboxylic acid là những hợp chất hữu cơ mà trong phân tử chứa nhóm carboxyl (-COOH) liên kết trực tiếp với nguyên tử carbon hoặc nguyên tử hydrogen.
Luyện tập 1 (SGK - tr.133)
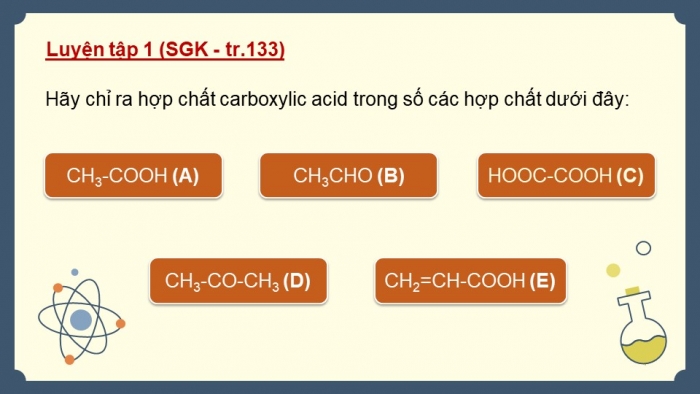
Hãy chỉ ra hợp chất carboxylic acid trong số các hợp chất dưới đây:
- Danh pháp
- Quan sát bảng 19.1 SGK tr. 133, rút ra cách gọi tên thay thế của monocarboxylic acid mạch hở.
- Nêu cách đánh số mạch chính đối với carboxylic acid mạch nhánh và carboxylic acid có mạch carbon không no. Cho ví dụ minh họa.
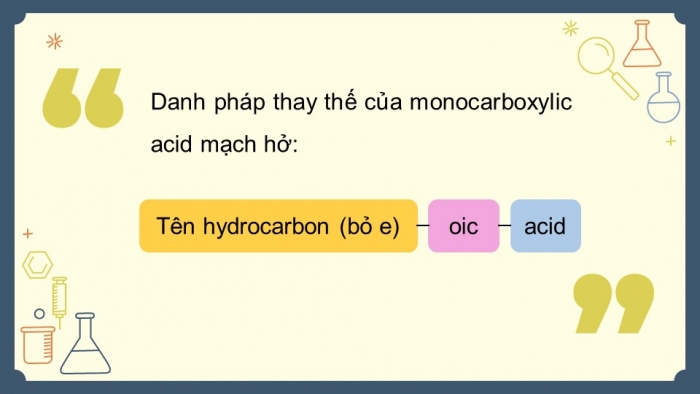
Danh pháp thay thế của monocarboxylic acid mạch hở:
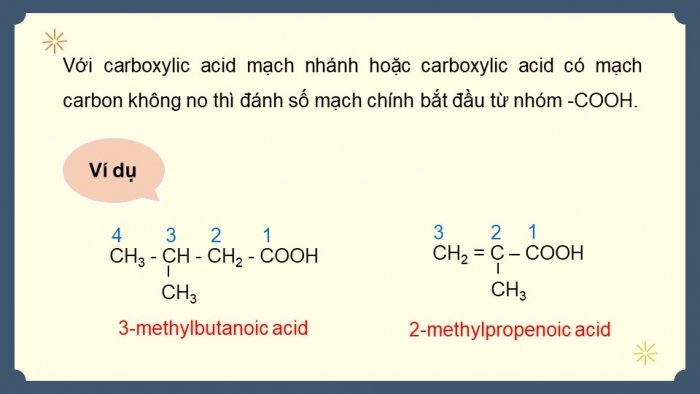
Với carboxylic acid mạch nhánh hoặc carboxylic acid có mạch carbon không no thì đánh số mạch chính bắt đầu từ nhóm -COOH.
Ví dụ
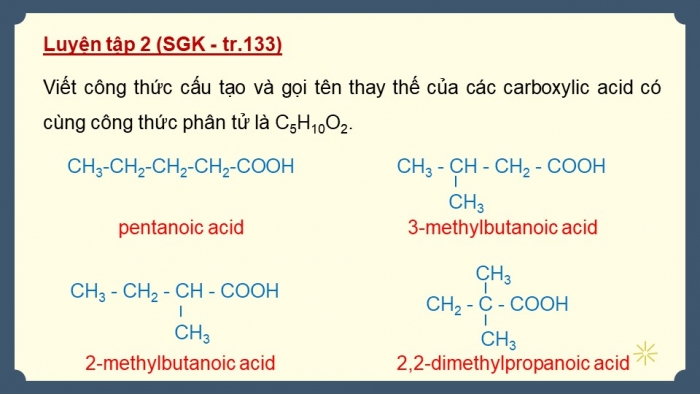
Luyện tập 2 (SGK - tr.133)
Viết công thức cấu tạo và gọi tên thay thế của các carboxylic acid có cùng công thức phân tử là C5H10O2.
pentanoic acid
3-methylbutanoic acid
2-methylbutanoic acid
2,2-dimethylpropanoic acid
- II. TÍNH CHẤT VẬT LÍ
Quan sát hình 19.1, đọc thông tin SGK và thực hiện yêu cầu:
Dự đoán ảnh hưởng của nhóm carboxyl đến tính chất vật lí của carboxylic acid.
Tạo được liên kết hydrogen nên có nhiệt độ sôi cao
Thảo luận nhóm đôi
Câu 1 (SGK - tr.134)
Căn cứ các dữ liệu về nhiệt độ sôi và nhiệt độ nóng chảy, hãy chỉ ra các carboxylic acid ở thể lỏng và ở thể rắn ở điều kiện thường.
|
Carboxylic acid |
(oC) |
Trạng thái |
|
HCOOH CH3COOH CH3CH2COOH CH3CH2CH2COOH CH3CH2CH2CH2COOH CH2=CH-COOH CH2=C(CH3)-COOH C6H5-COOH |
100,8 117,9 140,8 163,3 185,5 141,0 163,0 250,2 |
Lỏng Lỏng Lỏng Lỏng Lỏng Lỏng Lỏng Rắn |
Đọc hiểu nội dung mục II và trả lời các câu hỏi sau:
- Nhận xét về xu hướng biến đổi của nhiệt độ sôi của các carboxylic acid no, đơn chức, mạch hở theo chiều tăng dần của phân tử khối.
- So sánh nhiệt độ sôi của các carboxylic acid với các alcohol có cùng số nguyên tử carbon. Giải thích.
Tính chất vật lí
Ở nhiệt độ thường, các carboxylic acid ở thể lỏng hoặc thể rắn.
Nhiệt độ sôi của các carboxylic acid no, đơn chức, mạch hở đều tăng dần theo chiều tăng dần của phân tử khối.
Tan tốt trong nước. Khi số nguyên tử carbon trong phân tử tăng thì độ tan giảm dần.
Nhiệt độ sôi của carboxylic acid cao hơn của các alcohol có cùng số nguyên tử carbon.
Nguyên nhân do liên kết O-H trong nhóm carboxyl phân cực hơn liên kết O-H trong alcohol, dẫn đến liên kết hydrogen giữa các phân tử carboxylic acid bền vững hơn so với liên kết hydrogen hình thành giữa các phân tử alcohol.
Câu 2 (SGK - tr.134)
Vì sao acetic acid có thể tan vô hạn trong nước?
Nhờ khả năng tạo liên kết hydrogen với nước, các carboxylic acid đầu dãy như acetic acid tan vô hạn trong nước.
III TÍNH CHẤT HÓA HỌC
Hình ảnh về file sile, ppt trình chiếu






.....
=> Còn nữa.... Files tải về, sẽ có đầy đủ nội dung bài học
Nâng cấp lên tài khoản VIP để tải tài liệu và dùng thêm được nhiều tiện ích khác
Từ khóa tìm kiếm:
Bài giảng điện tử Hóa học 11 cánh diều, Tải giáo án Powerpoint Hóa học 11 cánh diều Bài 19: Carboxylic acid, Tải giáo án powerpoint Hóa học 11 cánh diều Bài 19: Carboxylic acid
