Tải giáo án Powerpoint Hóa học 10 KNTT bài 17: Biến thiên enthalpy trong các phản ứng hoá học
Tải giáo án trình chiếu hay còn gọi là giáo án powerpoint Hóa học 10 bộ sách Chân trời sáng tạo bài 17: Biến thiên enthalpy trong các phản ứng hoá học. Soạn giáo án được thiết kế với tiêu chí đẹp mắt, hiện đại kết hợp nhiều hoạt động, trò chơi, video học tập thú vị. Phương pháp giảng dạy mới kết hợp nhiều dạng bài tập phong phú sẽ giúp học sinh nắm chắc kiến thức trọng tâm bài học. Kéo xuống để tham khảo
Rõ nét về file powerpoint trình chiếu. => Xem thêm
CHƯƠNG 5: NĂNG LƯỢNG HOÁ HỌC
BÀI 17: BIẾN THIÊN ENTHALPY TRONG CÁC PHẢN ỨNG HOÁ HỌC
- KHỞI ĐỘNG
a
Phản ứng giữa đường glucose với oxygen tạo ra carbon dioxide, hơi nước và tỏa nhiều nhiệt. Sau khi chơi thể thao, cơ thể mệt mỏi, nghỉ ngơi vài phút, sau đó nếu một cốc nước hoa quả, em sẽ cảm thấy khỏe hơn. Có phải đường glucose đã “cháy” và cấp bù năng lượng cho cơ thể?
HÌNH ẢNH
- NỘI DUNG BÀI HỌC
- Phản ứng toả nhiệt, phản ứng thu nhiệt
- Biến thiên enthalpy của phản ứng
- Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành
- Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết
III. PHẦN TRIỂN KHAI KIẾN THỨC
- . Phản ứng toả nhiệt, phản ứng thu nhiệt
Em hãy đọc tình huống dưới đây và trả lời câu hỏi.
“Bạn Nam làm thí nghiệm:
(1) Thả thì vôi sống dạng bột (CaO) vào cốc 1 đựng nước cất.
(2) Thả C sủi vào cốc 2 chứa nước cất.
Nam thấy trước khi làm thí nghiệm, nhiệt độ của 2 cốc nước là 25oC. Cốc 1, sau khi cho vôi sống, nhiệt độ tăng lên 75oC. Cốc 2, sau khi thả C sủi, nhiệt độ giảm xuống 21oC.
Em hãy dự đoán thí nghiệm (1), (2) là phản ứng tỏa nhiệt hay thu nhiệt?
Đọc SGK và nêu khái niệm phản ứng toả nhiệt, phản ứng thu nhiệt.
Đáp án
Phản ứng (1) là phản ứng tỏa nhiệt, phản ứng (2) là phản ứng thu nhiệt.
Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt.
Phản ứng thu nhiệt là phản ứng hấp thu năng lượng dưới dạng nhiệt.
Em hãy đọc Câu hỏi 1 và trả lời câu hỏi.
- Khi đun nóng ống nghiệm đựng KmnO4 (thuốc tím), nhiệt của ngọn lửa làm cho KMnO4bị nhiệt phân, tạo hỗn hợp bột màu đen:
2KMnO4 → K2MnO4 + MnO2 + O2
Em hãy dự đoán phản ứng này toả nhiệt hay thu nhiệt.
Đáp án:
Em dự đoán phản ứng này thu nhiệt vì em thấy phản ứng nhiệt phân KMnO4 cần cung cấp nhiệt độ.
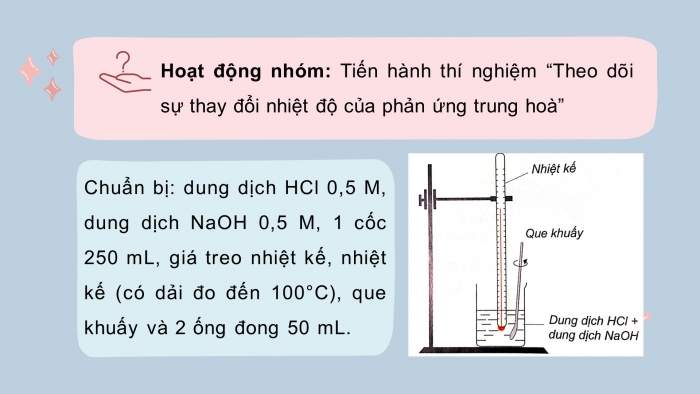
Hoạt động nhóm: Tiến hành thí nghiệm “Theo dõi sự thay đổi nhiệt độ của phản ứng trung hoà”
Chuẩn bị: dung dịch HCl 0,5 M, dung dịch NaOH 0,5 M, 1 cốc 250 mL, giá treo nhiệt kế, nhiệt kế (có dải đo đến 100°C), que khuấy và 2 ống đong 50 mL.
Tiến hành:
- Dùng ống đong lấy 50 mL dung dịch HCl 0,5 M cho vào cốc phản ứng, lắp nhiệt kế lên giá sao cho đầu nhiệt kế nhúng vào dung dịch trong cốc (Hình 17.1). Đọc nhiệt độ dung dịch.
- Dùng ống đong khác lấy 50 mL dung dịch NaOH 0,5 M cho vào cốc phản ứng. Khuấy nhẹ.
HÌNH 17.1
Theo dõi sự thay đổi nhiệt độ của dung dịch và trả lời câu hỏi:
- Nhiệt độ trên nhiệt kế thay đổi như thế nào sau khi rót dung dịch NaOH vào cốc? Phản ứng trung hoà là toả nhiệt hay thu nhiệt?
- Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ thay đổi như thế nào so với thí nghiệm trên?
Đáp án
- Sau khi rót dung dịch NaOH vào cốc thì nhiệt độ trên nhiệt kế tăng dần.
⇒ Phản ứng tỏa nhiệt.
- Nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ sau phản ứng vẫn tăng nhưng tăng ít hơn so với thí nghiệm trên.
- Biến thiên enthalpy của phản ứng
2.1. Biến thiên enthalpy
Em hãy đọc nội dung SGK và nêu khái niệm biến thiên enthalpy
Ở điều kiện áp suất không đổi, nhiệt lượng tỏa ra hay thu vào của phản ứng gọi là biến thiên enthalpy của phản ứng.
2.2. Biến thiên enthalpy chuẩn
Em hãy tìm hiểu nội dung SGK và trả lời các câu hỏi
Biến thiên enthalpy của các phản ứng phụ thuộc vào gì?
Biến thiên enthalpy chuẩn là gì?
Đáp án:
- Biến thiên enthalpy của các phản ứng phụ thuộc vào điều kiện xảy ra phản ứng (như nhiệt độ, áp suất) và trạng thái vật lí của các chất.
- Biến thiên enthalpy chuẩn là nhiệt toả ra hay thu vào của phản ứng được xác định ở điều kiện chuẩn: áp suất 1 bar (đối với chất khí), nồng độ 1 mol/L (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 25oC (298K), kí hiệu ∆r
2.3. Ý nghĩa của biến thiên enthalpy
∆rH > 0: Phản ứng thu nhiệt.
∆rH < 0: Phản ứng tỏa nhiệt.
Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì lượng nhiệt tỏa ra hay thu vào vủa phản ứng càng nhiều.
Em hãy trả lời câu hỏi 2, 3 SGK trang 83
- Cho các phương trình nhiệt hoá học:
(1) CaCO3(s) CaO(s) + CO2(g)
(2) C2H4(g) + H2(g) C2H6(g)
(3) Fe2O3(s) + 2Al(s) Al2O3(s) + 2Fe(s)
Trong các phản ứng trên, phản ứng nào toả nhiệt, phản ứng nào thu nhiệt?
- Biết phản ứng đốt cháy khí carbon monoxide (CO) như sau:
CO(s) + O2(g) CO2(g)
Ở điều kiện chuẩn, nếu đốt cháy hoàn toàn 2,479 L CO thì nhiệt lượng toả ra là bao nhiêu?
- 4. Phản ứng tôi vôi toả ra nhiệt lượng rất lớn, có thể làm sôi nước. Hãy nêu các biện pháp để đảm bảo an toàn khi thực hiện quá trình tôi vôi.
Đáp án
Ta có: > 0 Phản ứng thu nhiệt
< 0 Phản ứng toả nhiệt
Phản ứng (1) là phản ứng thu nhiệt; Phản ứng (2) và (3) là phản ứng thu nhiệt.
Phản ứng đốt cháy 1 mol hay 24,79L khí carbon monoxide (CO) tỏa ra nhiệt lượng 283kJ.
⇒ Nếu đốt cháy hoàn toàn 2,479 L khí CO thì nhiệt lượng toả ra là
- = 28,3 kJ
Hình ảnh về file sile, ppt trình chiếu











.....
=> Còn nữa.... Files tải về, sẽ có đầy đủ nội dung bài học
Nâng cấp lên tài khoản VIP để tải tài liệu và dùng thêm được nhiều tiện ích khác
Từ khóa tìm kiếm:
Giáo án Powerpoint Hóa học 10 Kết nối, giáo án điện tử Hóa học 10 KNTT bài 17: Biến thiên enthalpy trong các phản, giáo án trình chiếu Hóa học 10 kết nối bài 17: Biến thiên enthalpy trong các phản
