Tải giáo án Powerpoint KHTN 8 KNTT Bài 11: Muối
Tải bài giảng điện tử powerpoint khoa học tự nhiên 8 kết nối tri thức Bài 11: Muối. Bài học được thiết kể đẹp mắt, nội dung giảng dạy hay nhiều trò chơi và video phong phú thu hút học sinh tập trung nắm bắt kiến thức quan trong. Giáo án tải về chỉnh sửa được. Kéo xuống để xem chi tiết
Rõ nét về file powerpoint trình chiếu. => Xem thêm
CHÀO MỪNG CÁC EM ĐẾN VỚI TIẾT HÓA HỌC!
KHỞI ĐỘNG
Muối ăn (NaCl)
> Đóng vai trò vô cùng quan trọng đối với hoạt động trao đổi chất của con người.
Đá vôi (CaCO3)
> Dùng để sản xuất vôi sống, làm đường, làm bê tông, chất độn trong sản xuất cao su, xà phòng,…
Diêm tiêu (KNO3)
> Sử dụng để chế tạo thuốc nổ đen, bảo quản thực phẩm, điều chế oxygen trong phòng thí nghiệm.
Muối ăn, đá vôi hay diêm tiêu đều là muối. Vậy muối là gì, chúng có tính chất hóa học như thế nào?
BÀI 11. MUỐI
NỘI DUNG BÀI HỌC
Khái niệm
Tính tan của muối
Tính chất hoá học
Điều chế
Mối quan hệ giữa các hợp chất vô cơ
- KHÁI NIỆM
THẢO LUẬN NHÓM
|
BẢNG 11.1. PHẢN ỨNG TẠO THÀNH MUỐI, TÊN GỌI VÀ THÀNH PHẦN PHÂN TỬ CỦA MỘT SỐ MUỐI |
|||
|
Phản ứng |
Công thức phân tử của muối tạo thành và tên gọi |
Thành phần phân tử của muối tạo thành |
|
|
Cation kim loại |
Anion gốc acid |
||
|
Kim loại + Acid → Muối + Hydrogen Zn + 2HCl → ZnCl2 + H2 |
ZnCl2 Zinc chloride |
Zn2+ |
Cl- |
|
Acid + Base → Muối + Nước H2SO4 + Cu(OH)2 → CuSO4 + 2H2O |
CuSO4 Copper(II) sulfate |
Cu2+ |
|
|
Acid + Oxide base → Muối + Nước H2SO4 + FeO → FeSO4 + H2O |
FeSO4 Iron(II) sulfate |
Fe2+ |
|
Em hãy quan sát Bảng 11.1 và thực hiện các yêu cầu sau:
- Nhận xét về sự khác nhau giữa thành phần phân tử của acid (chất phản ứng) và muối (chất sản phẩm). Đặc điểm chung của các phản ứng ở Bảng 11.1 là gì?
- Nhận xét về cách gọi tên muối.
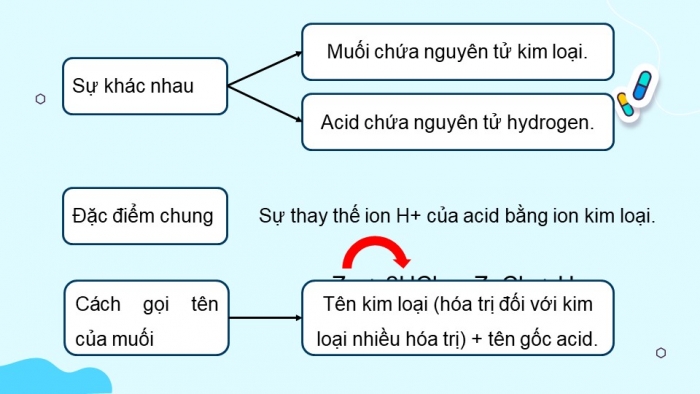
Sự khác nhau
- Muối chứa nguyên tử kim loại.
- Acid chứa nguyên tử hydrogen.
Đặc điểm chung
- Sự thay thế ion H+ của acid bằng ion kim loại.
Cách gọi tên của muối
Zn + 2HCl → ZnCl2 + H2
Tên kim loại (hóa trị đối với kim loại nhiều hóa trị) + tên gốc acid.
Thành phần phân tử của acid và muối khác nhau ở chỗ muối chứa nguyên tử kim loại và acid chứa nguyên tử hydrogen.
Đặc điểm chung của các phản ứng ở bảng 11.1 là sự thay thế ion H+ của acid bằng ion kim loại.
Cách gọi tên của muối: tên kim loại (hóa trị đối với kim loại nhiều hóa trị) + tên gốc acid.
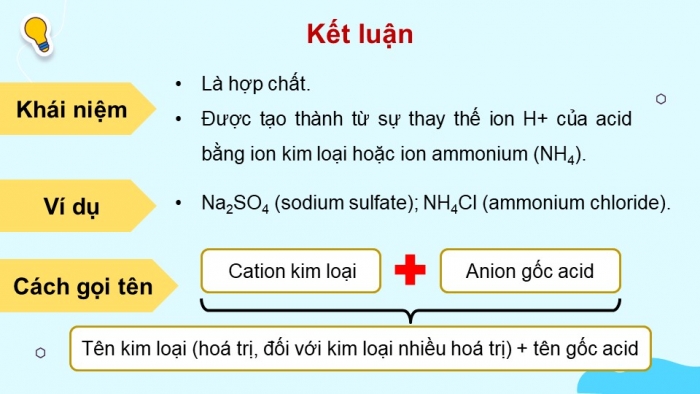
Kết luận
Khái niệm
- Là hợp chất.
- Được tạo thành từ sự thay thế ion H+ của acid bằng ion kim loại hoặc ion ammonium (NH4).
Ví dụ
- Na2SO4 (sodium sulfate); NH4Cl (ammonium chloride).
Cách gọi tên
Cation kim loại
Anion gốc acid
Tên kim loại (hoá trị, đối với kim loại nhiều hoá trị) + tên gốc acid
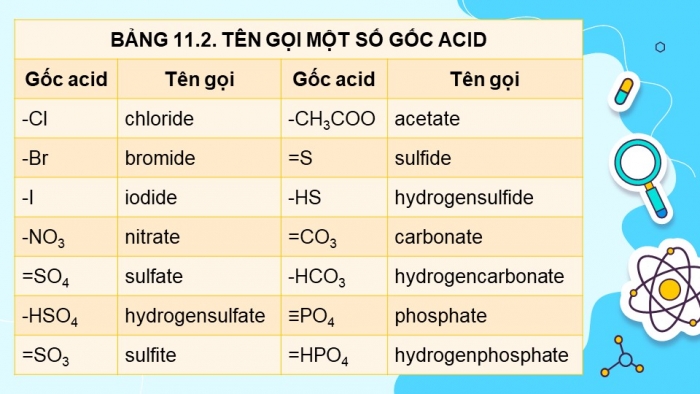
|
BẢNG 11.2. TÊN GỌI MỘT SỐ GỐC ACID |
|||
|
Gốc acid |
Tên gọi |
Gốc acid |
Tên gọi |
|
-Cl |
chloride |
-CH3COO |
acetate |
|
-Br |
bromide |
=S |
sulfide |
|
-I |
iodide |
-HS |
hydrogensulfide |
|
-NO3 |
nitrate |
=CO3 |
carbonate |
|
=SO4 |
sulfate |
-HCO3 |
hydrogencarbonate |
|
-HSO4 |
hydrogensulfate |
≡PO4 |
phosphate |
|
=SO3 |
sulfite |
=HPO4 |
hydrogenphosphate |
Em hãy hoàn thành câu hỏi mục I – SGK tr.49 và Phiếu học tập số 1:
- Viết công thức của các muối sau: potassium sulfate, sodium hydrogensulfate, sodium hydrogencarbonate, sodium chloride, sodium nitrate, calcium hydrogenphosphate, magnesium sulfate, copper(II) sulfate.
- Gọi tên các muối sau: AlCl3, KCl, Al2(SO4)3, MgSO4, NH4NO3, NaHCO3.
- Viết phương trình hoá học của phản ứng tạo thành muối KCl và MgSO4.
Câu 1
|
Tên gọi muối |
Công thức |
|
potassium sulfate |
K2SO4 |
|
sodium hydrogensulfate |
NaHSO4 |
|
sodium hydrogencarbonate |
NaHCO3 |
|
sodium chloride |
NaCl |
|
sodium nitrate |
NaNO3 |
|
calcium hydrogenphosphate |
CaHPO4 |
|
magnesium sulfate |
MgSO4 |
|
copper(II) sulfate |
CuSO4 |
Câu 2
|
Muối |
Tên các muối |
|
AlCl3 |
aluminium chloride |
|
KCl |
potassium chloride |
|
Al2(SO4)3 |
aluminium sulfate |
|
MgSO4 |
magnesium sulfate |
|
NH4NO3 |
ammonium nitrate |
|
NaHCO3 |
sodium hydrocarbonate |
Câu 3
Phản ứng tạo muối KCl:
KOH + HCl -> KCl + H2O
Phản ứng tạo muối MgSO4:
Mg + H2SO4 -> MgSO4 + H2
PHIẾU HỌC TẬP SỐ 1
Hình ảnh về file sile, ppt trình chiếu









.....
=> Còn nữa.... Files tải về, sẽ có đầy đủ nội dung bài học
TẢI GIÁO ÁN POWERPOINT BẢN ĐẦY ĐỦ:
- Giáo án powerpoint, dễ dàng chỉnh sửa nếu muốn
- Sinh động, hiện đại, đẹp mắt để tạo hứng thú học cho học sinh
- Giáo án có đủ Lí + Hóa + sinh
THỜI GIAN BÀN GIAO GIÁO ÁN:
Nhận đủ cả năm ngay sau thanh toán
PHÍ GIÁO ÁN:
- Word: 500k/kì - 550k/cả năm
- Powerpoint: 600k/kì - 700k/cả năm
- Word + Powerpoint: 800k/kì - 900k/cả năm
=> Tặng kèm nhiều tài liệu tham khảo khi mua giáo án:
- Đề thi
- Trắc nghiệm
CÁCH ĐẶT TRƯỚC:
- Bước 1: gửi phí vào tk: 10711017 - Chu Văn Trí - Ngân hàng ACB (QR)
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo đặt trước
Từ khóa tìm kiếm:
Bài giảng điện tử khoa học tự nhiên 8 KNTT, giáo án điện tử khoa học tự nhiên 8 kết nối Bài 11: Muối, giáo án powerpoint khoa học tự nhiên 8 kết nối tri thức Bài 11: Muối
