Tải giáo án Powerpoint KHTN 8 KNTT Bài 5: Định luật bảo toàn khối lượng và phương trình hoá học
Tải bài giảng điện tử powerpoint khoa học tự nhiên 8 kết nối tri thức Bài 5: Định luật bảo toàn khối lượng và phương trình hoá học. Bài học được thiết kể đẹp mắt, nội dung giảng dạy hay nhiều trò chơi và video phong phú thu hút học sinh tập trung nắm bắt kiến thức quan trong. Giáo án tải về chỉnh sửa được. Kéo xuống để xem chi tiết
Rõ nét về file powerpoint trình chiếu. => Xem thêm
THÂN MẾN CHÀO CÁC EM HỌC SINH ĐẾN VỚI BÀI HỌC MỚI
KHỞI ĐỘNG
Khi các phản ứng hóa học xảy ra, lượng các chất phản ứng giảm dần. Lượng các chất sản phẩm tăng dần. Vậy tổng khối lượng các chất trước và sau phản ứng có thay đổi hay không ?
BÀI 5 - ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG VÀ PHƯƠNG TRÌNH HÓA HỌC
NỘI DUNG BÀI HỌC
Định luật bảo toàn khối lượng
Phương trình hóa học
01 ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG
- Nội dung định luật bảo toàn khối lượng
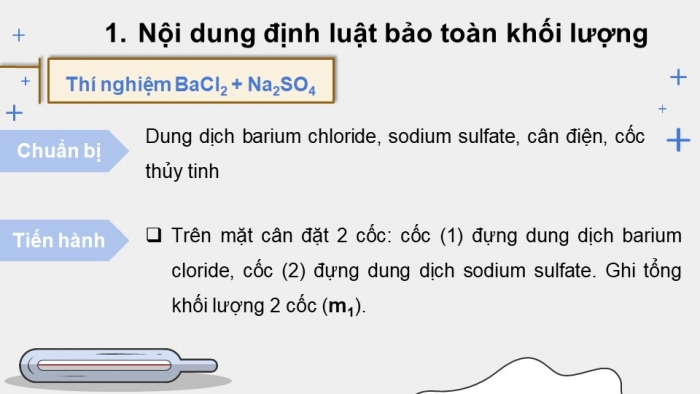
Thí nghiệm BaCl2 + Na2SO4
Chuẩn bị
Dung dịch barium chloride, sodium sulfate, cân điện, cốc thủy tinh
Tiến hành
- Trên mặt cân đặt 2 cốc: cốc (1) đựng dung dịch barium cloride, cốc (2) đựng dung dịch sodium sulfate. Ghi tổng khối lượng 2 cốc (m1).
- Đổ cốc (1) vào cốc (2), lắc nhẹ để hai dung dịch trộn lẫn với nhau. Quan sát thấy có một chất rắn xuất hiện ở cốc (2). Phản ứng xảy ra như sau:
- Barium chloride + Sodium sulfate → Barium sulfate + Sodium chloride.
- Đặt hai cốc trở lại mặt cân. Ghi khối lượng (m2).
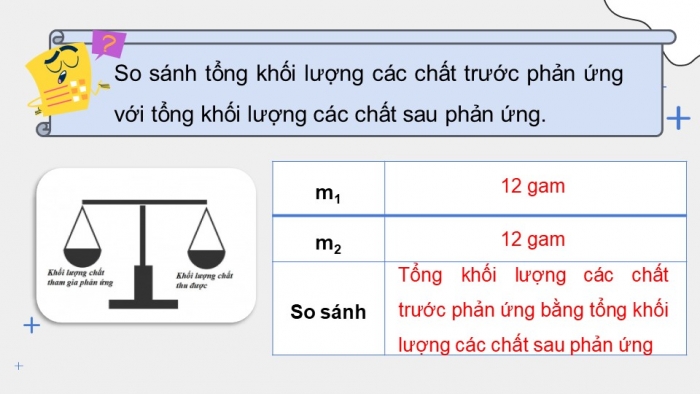
So sánh tổng khối lượng các chất trước phản ứng với tổng khối lượng các chất sau phản ứng.
|
m1 |
|
|
m2 |
|
|
So sánh |
|
LỊCH SỬ RA ĐỜI CỦA ĐỊNH LUẬT BẢO TOÀN KHỐI LƯỢNG
Khi cân bình nút kin đựng bột kim loại trước và sau khi nung, M.V. Lomonosov nhận thấy rằng khối lượng của chúng không thai đổi, mặc dù những chuyển hóa hóa học đã xảy ra với kim loại trong bình. Khi áp dụng các phương pháp định lượng nghiên cứu phản ứng hóa học, năm 1748, M.V. Lomonosov đã tìm ra được một trong những định luật quan trong nhất của tự nhiên, mang tên định luật bảo toàn khối lượng. Ông trình bày định luật đó như sau: “Tất cả những biến đổi xảy ra trong tự nhiên thực chất là nếu lấy đi bao nhiêu ở vật thể này, thì có bấy nhiêu được thêm vào ở vật thể khác. Như vậy, nếu ở đây giảm đi bao nhiêu vật chất, thì sẽ có từng đấy vật chất tăng lên ở chỗ khác”. Cùng thời điểm đó A.L. Lavoisier cũng tiến hành được thí nghiệm độc lập chứng minh được sự bảo toàn khối lượng trong các phản ứng hóa học.
Hãy quan sát hình ảnh sau kết hợp đọc thông tin trong sgk, hãy giải thích cơ sở của định luật bảo toàn khối lượng và trả lời câu hỏi mục I.1 sgk trang 25: sau khi đốt cháy than tổ ong (thành phần chính là carbon) thì thu được xỉ than. Xỉ than nặng hơn hay nhẹ hơn than tổ ong? Giải thích.
Giải thích
Trong các phản ứng hóa học, chỉ có liên kết giữa các nguyên tử thay đổi, còn số nguyên tử của mỗi nguyên tố hóa học vẫn giữ nguyên, vì vậy tổng khối lượng của các chất tham gia phản ứng bằng tổng khối lượng của các sản phẩm.
Đáp án câu hỏi 1
Trong sơ đồ phản ứng, số nguyên tử C trước và sau phản ứng đều là 1, số nguyên tử O trước và sau phản ứng đều là 2, do đó khối lượn chúng khống thay đổi, nghĩa là khối lượng carbon di oxide bằng tổng khối lượng của carbon và oxygen.
- Áp dụng định luật bảo toàn khối lượng
VD: Biết khối lượng barium chloride và sodium sulfate đã phản ứng lần lượt lad 20,8 gam và 14,2 gam, khối lượng của bari sulfate tạo thành là 23,3 gam. Khối lượng sodium chloride tạo thành là bao nhiêu?
Theo định luật bảo toàn khối lượng ta có:
mBari chloride + mSodium sulfate = mBari sulfate + mSodium chloride
20,8 + 14,2 -23,3 = 11,7 (g)
Tổng quát: Nếu trong phản ứng có n chất, khi biết khối lượng đã tham gia và tạo thành của (n-1) chất, ta sẽ xác định được khối lượng của chất còn lại.
PHIẾU HỌC TẬP SỐ 1
Câu 1: Sau khi đốt cháy than tổ ong ( thành phần chính là carbon) thì thu được xỉ than. Xỉ than nặng hơn hay nhẹ hơn than tổ ong? Giải thích.
Câu 2: Vôi sống (calcium oxide) phản ứng với một số chất có mặt trong không khí như sau:
Calcium oxide + Carbon dioxide → Calcium carbonate
Calcium oxide + nước → Calcium hydroxide
Khi làm thí nghiệm, một học sinh quên đậy nắp lọ đựng vôi sống, sau một thời gian khối lượng của lọ sẽ thay đổi như thế nào?
Câu 3: Cho 5,6 gam sắt (iron) tác dụng vừa đủ với 7,3g hydrochloric acid, thu được 12,7 gam iron (II) chloride và khí hydrogen. Tính khối lượng hydrogen tạo thành.
Câu 4: Đốt cháy hoàn toàn 12 gam carcon trong không khí thu được 44g khí carbon dioxide. Tính khối lượng khí oxygen đã tham gia phản ứng.
ĐÁP ÁN PHIẾU HỌC TẬP SỐ 1
Câu 1: Xỉ than nhẹ hơn than tổ ong vì phần carbon trong than tổ ong đã phản ứng với khí oxygen trong không khí thành chất khí carbon dioxide và đi vào không khí.
Câu 2: Khối lượng lọ đựng vô sống tăng lên vì vôi sống đã pản ứng với hơi nước và carbon dioxide có trong không khí tạo thành các chất rắn trong lọ. Khối lượng lọ tăng lên bằng khối lượng carbon dioxide và hơi nước.
Câu 3:
Theo định luật bảo toàn khối lượng ta có:
miron + mHydrochloric acid = mirone (II) chloride + mHydrogen
mHydrogen = 5,6 + 7,3 - 12,7 = 0,2 (g)
Câu 4:
Theo định luật bảo toàn khối lượng ta có:
mcarbon + moxygen = mcarbon dioxide
moxygen = 44 - 12 = 32 (g)
02 PHƯƠNG TRÌNH HÓA HỌC
- Lập phương trình hóa học
Ví dụ 1
Phản ứng giữa oxygen và hydrogen:
Khí hydrogen + Khó oxygen → Nước
Thay thế tên chất bằng công thức hóa học, ta có:
H2 + O2 → H2O
Vì số nguyên tử của mỗi nguyên tố ở hai vế của sơ đồ phản ứng bằng nhau, nên ta thêm các hệ số đứng trước chất, ta được phương trình hóa học:
2H2 + O2 → 2H2O
Phương trình hóa học biểu diễn ngắn gọn phản ứng hóa học.
Ví dụ 2
Viết PTHH phản ứng giữa alumminium và oxygen.
Các bước lập phương trình hóa học:
- Bước 1: Viết sơ đồ phản ứng.
Al + O2 → Al2O3
- Bước 2: Cân bằng số nguyên tử của mỗi nguyên tố ở 2 vế.
Al + 3O2 → 2Al2O3
- Bước 3: Viết phương trình hóa học của phản ứng.
4Al + 3O2→ 2Al2O3
LƯU Ý
Hình ảnh về file sile, ppt trình chiếu









.....
=> Còn nữa.... Files tải về, sẽ có đầy đủ nội dung bài học
TẢI GIÁO ÁN POWERPOINT BẢN ĐẦY ĐỦ:
- Giáo án powerpoint, dễ dàng chỉnh sửa nếu muốn
- Sinh động, hiện đại, đẹp mắt để tạo hứng thú học cho học sinh
- Giáo án có đủ Lí + Hóa + sinh
THỜI GIAN BÀN GIAO GIÁO ÁN:
Nhận đủ cả năm ngay sau thanh toán
PHÍ GIÁO ÁN:
- Word: 500k/kì - 550k/cả năm
- Powerpoint: 600k/kì - 700k/cả năm
- Word + Powerpoint: 800k/kì - 900k/cả năm
=> Tặng kèm nhiều tài liệu tham khảo khi mua giáo án:
- Đề thi
- Trắc nghiệm
CÁCH ĐẶT TRƯỚC:
- Bước 1: gửi phí vào tk: 10711017 - Chu Văn Trí - Ngân hàng ACB (QR)
- Bước 2: Nhắn tin tới Zalo Fidutech - nhấn vào đây để thông báo đặt trước
Từ khóa tìm kiếm:
Bài giảng điện tử khoa học tự nhiên 8 KNTT, giáo án điện tử khoa học tự nhiên 8 kết nối Bài 5: Định luật bảo toàn khối lượng, giáo án powerpoint khoa học tự nhiên 8 kết nối tri thức Bài 5: Định luật bảo toàn khối lượng
